近日,专注于RNA干扰(RNAi)技术开发及小核酸药物产业化的苏州瑞博生物技术股份有限公司(以下简称“瑞博生物”),连续对外披露两轮融资,一笔为3300万美元,另一笔超过2亿元。再次引发行业对于小核酸药物市场的广泛关注。
小核酸药物被认为“现代制药的第三次浪潮”,今天我们从小核酸药物的发展、研究现状等方面深入了解一下小核酸药物赛道。
PART 01
小核酸药物发展历程
小核酸药物是一类由十几个到几十个核苷酸组成的短链核酸药物,它们通过干预靶标基因的表达,在mRNA水平上实现对疾病的治疗,是一种“既治标又治本”的治疗方式,具有高效性、特异性和长期性等优势。主要包括反义核酸(ASO)、小干扰RNA(siRNA)、微小RNA(miRNA)等类型。
小核酸大概可以分为以下三个阶段,1970-2006年的萌芽阶段;2006-2016年的震荡发展期;随后进入了快速发展期。
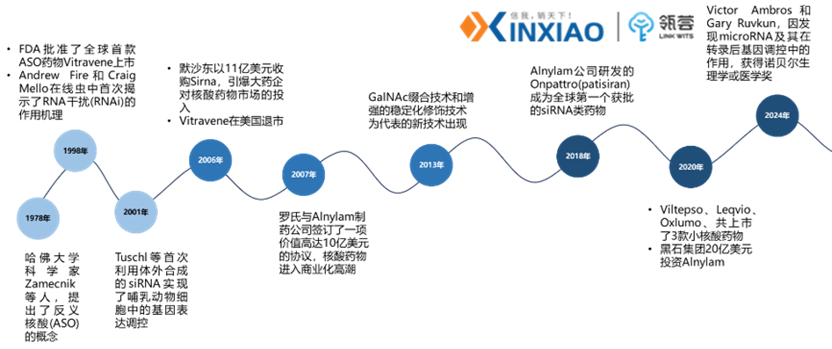
1978年,哈佛大学科学家Zamecnik等人首次发现用一段互补的核苷酸链可以抑制RSV病毒的复制活动,提出了反义核酸(ASO)的概念,为核酸药物奠定的理论基础。
1998年,FDA批准了全球首款ASO药物Vitravene上市,用于治疗艾滋病患者的眼部CMV病毒感染。同年,Andrew Fire和Craig Mello在线虫中首次揭示了RNA干扰(RNAi)的作用机理,这一发现使他们在2006年荣获诺贝尔生理学或医学奖。
2006年,默沙东以11亿美元收购Sirna,罗氏与Alnylam签订价值高达10亿美元的技术合作协议,2014年,默沙东将Sirna以低于原收购价出售给Alnylam。
2018年,Alnylam公司研发的Onpattro (patisiran)成为全球第一个获批的siRNA类药物,用于治疗由hATTR引起的多发性神经病。
疫情期间,辉瑞-BioNTech和Moderna的mRNA疫苗的速度获批,也直接推动了整个核酸药物领域的快速发展。
PART 02
截至目前,全球已获批的小核酸药物有22款,包括12款ASO药物、7款siRNA药物、2款配体类药物以及1个寡核苷酸端粒酶抑制剂。其中Vitravene、Macugen、Kynamro三款产品因药品安全性问题或市场竞争等因素已退市。
全球已上市小核酸药物汇总

备注:手动统计,如有遗漏,请指正
根据国家药品评审中心(CDE)数据,截至发稿前,国内仅获批了两款进口的小核酸药物。2019年4月,国家药监局批准了诺西那生钠(Nusinersen)的上市申请,用于治疗脊髓性肌萎缩症(SMA);2024年10月,又批准了托夫生(Tofersen)的上市申请。
全球共计约900家企业正在研发与核酸相关的药物,管线高达2600条,其中罕见病药物占比较高,达13.76%,70%的项目正处于临床前期阶段。
全球核酸药物管线适应症分布情况
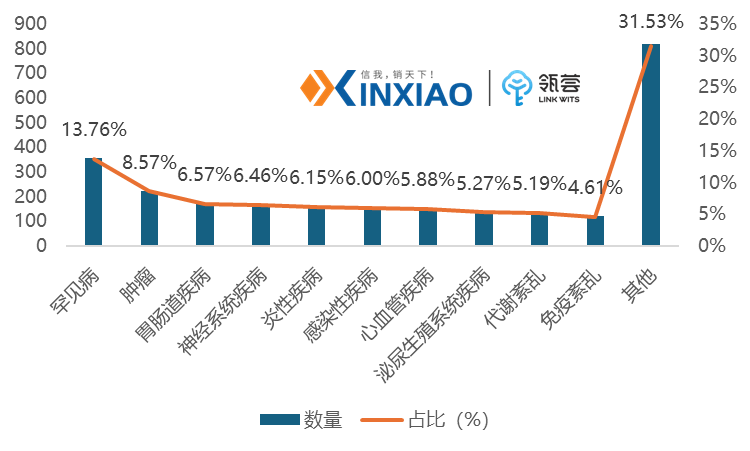
数据来源:药智网,信销行研整理
PART 03
小核酸药物市场潜力:Spinraza2024年营收15.73亿美元位列榜首
根据已上市小核酸药物企业公开的资料显示,2024年小核酸药物市场销售额持续增长,总营收近51亿美元,同比增长12%。
2018-2024年全球小核酸药物市场销售额(亿美元)
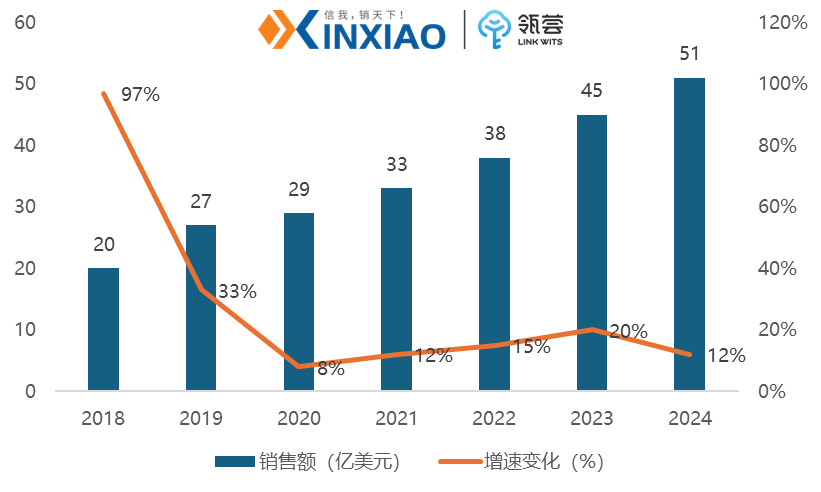
数据来源:公开渠道,信销行研整理
小核酸药物中,针对脊髓性肌萎缩症的 Spinraza 商业化最为成功,2024年Spinraza的销售额达15.73亿美元,累计全球销售额近 138 亿美元。Amvuttra(Vutrisiran)2024 年销售额为9.71亿美元,同比增长约 73%,排名第二。
2024年部分小核酸药物销售额

数据来源:公开渠道,信销行研整理
PART 03
虽然国际企业Lonis、Alnylam、Dicerna、Sarepta Therapeutics等公司在小核酸药物赛道处于领先地位,近年中国药企在小核酸赛道也取得了较大的进展。
中国已有近200家企业布局这一领域,瑞博生物、艾博生物、舶望制药、海昶生物等企业均有产品进入临床阶段,未来3年有望国产药品上市。
国内目前已有治疗高血脂、慢性乙肝等3款小核酸产品进入临床Ⅲ期:
维亚臻生物技术(香港)有限公司VSA-003,是一款siRNA,该药物可通过LDLR 非依赖性及依赖性双重降脂机制,有效降低HoFH患者LDL-C水平。
AHB-137是浩博医药研发的针对慢性乙型肝炎临床治愈的非偶联型的反义寡核苷酸(ASO)药物。近日,浩博医药对外公布AHB-137取得了较好的临床结果,在24周治疗组中,75%(24/32)的受试者达到了这一主要终点;在16周治疗组中,66%(21/32)的受试者达到了这一主要终点。在达到主要终点的受试者中,超过80%的受试者在治疗12周内实现了HBsAg的清除,并且在治疗结束时,24周和16周组分别有54%和33%的受试者出现了乙肝表面抗体(anti-HBs)的血清转换。
瑞博生物的RBD1007已进入Ⅲ期临床,用于治疗非动脉炎性前部缺血性视神经病变。
另外,已有多家中国药企的小核酸药物通过对外授权的方式,快速推进全球化进程。
2024 年 1 月,舶望将 1/2a 期心血管产品大中华区以外权益、1 期心血管产品的全球权益以及最多两个心血管靶点药物许可选择权授权给诺华,获得 1.85 亿美元预付款,潜在里程碑最高 42 亿美元。
2025年6月,靖因药业将新一代长效凝血因子XI(FXI)靶向小干扰RNA(siRNA)疗法SRSD107授权给CRISPR Therapeutics,获得首付款9500万美元,并有资格获得超8亿美元的预付款和里程碑付款。
随着技术突破和临床验证,核酸药物有望在未来十年迎来爆发式增长,为全球患者带来更多突破性治疗方案。