在创新药的研发竞赛中,时间与资金是两大关键变量。过去,审评审批的不确定性与市场回报的未知性,如同悬在药企头顶的“达摩克利斯之剑”。然而,2025年一系列国家级政策的重磅出台,正在系统性地移除这些障碍,为中国制药产业注入了前所未有的“确定性”,推动整个行业向高质量与全球化方向“换档”提速。

一、向内赋能:全链条政策组合拳构建研发“高速路”
这种确定性首先体现在研发与市场准入效率的飞跃上。2025年年中,国家医保局与国家卫健委联合印发的 《支持创新药高质量发展的若干措施》,其意义远超一次普通的文件更新。它是一套覆盖“研、审、用、付”全周期的系统工程。
在研发起点,政策开始提供“精准导航”。国家医保局探索利用全国统一的医保信息平台,进行疾病谱与临床需求的数据分析,为药企确定研发方向、避免同质化内卷提供参考。这标志着监管角色从单纯的审批者,开始向产业生态的协同共建者转变。同时,国家药监局推出的“30日创新药临床试验快速审评通道”,将关键环节的审批时限从60个工作日压缩一半,为真正具有临床价值的药物研发按下了加速键。
在商业化终点,政策则着力铺设“多元轨道”。长期以来,创新药面临“入院难、支付难”的“最后一公里”问题。本次政策明确规定,医疗机构不得以药占比、用药目录数量等为由影响创新药配备,并鼓励及时召开药事会,这直接破除了关键的进院壁垒。更革命性的举措在于支付体系的扩容——建立商业健康保险创新药品目录。这相当于在“保基本”的基本医保之外,为临床价值高、价格也较高的创新药开辟了一条市场化的“双轨制”支付通道,让创新回报机制更加清晰和可持续。地方层面也迅速跟进,例如北京出台的32条新举措中,甚至将药品补充申请的审评时限从200个工作日压缩至60个,极大地加快了上市药品的技术迭代。
这一系列环环相扣的政策,直接目的就是引导行业告别“内卷式”的“伪创新”,转而投向具备高临床价值的“真创新”,将资金与人才引向正确的方向。

二、向外联通:主动融入全球规则,为“中国创新”铺就出海航道
如果说内部政策为创新提供了沃土,那么对接国际规则则是中国创新药走向全球市场的“通行证”。2025年,中国在药品监管国际化上迈出了决定性步伐。
最核心的信号是,国家药监局明确将于2026年3月31日后全面适用国际人用药品注册技术协调会(ICH)的E6(R3)《药物临床试验质量管理规范》指导原则。这不仅是技术标准的升级,更是监管理念的革新。E6(R3)强调“以患者为中心”和“基于风险的质量管理”。其全面实施意味着,在中国开展的临床试验数据质量和伦理规范,将获得美国FDA、欧盟EMA等全球主要监管机构的无差别认可,从根本上解决了中国创新药出海的“数据互信”问题,为开展国际多中心临床试验(MRCT)扫清了障碍。
与此同时,国家层面也在积极搭建实质性的出海服务平台。中国—东盟区域医药交易(集采)平台的正式运行具有标杆意义。该平台由国家和地方共建,已吸引114家中国头部药企和10家国外采购商入驻,提供从信息展示、交易撮合到跨境结算的全流程服务。杭州中美华东制药通过该平台完成了首单对新加坡的跨境线上交易,验证了这条“官方直通车”的高效与可靠。这不仅仅是卖出了几盒药,更标志着一种可复制的、标准化的出海通道正在形成,尤其为大量优质的中小型药企和“小而美”的医药项目降低了国际化门槛。

三、趋势前瞻:在确定的轨道上,产业将驶向何方?
清晰的政策导向与稳定的规则预期,正在重塑产业的投资逻辑与研发策略。未来几年,中国制药领域将呈现出几个明确的趋势:
· 研发趋势:从“泛创新”到“深水区”与全球化前瞻布局
在政策引导下,资金将更聚焦于真正解决未满足临床需求的领域,如重大传染病、罕见病、儿童用药等。同时,由于国内临床数据国际认可度提升,药企在立项之初便会更多考虑全球市场潜力,开展国际多中心临床试验(MRCT)将成为头部创新药企的“标准动作”。前沿技术方面,AI与制药的融合将深化。北京等地的政策已明确鼓励设立AI研发中心,推动AI在靶点发现、化合物筛选等环节的应用。建设高质量、标准化的生物样本库,也为基于真实世界数据的精准研发奠定了基础。
· 交易与合作趋势:跨境授权(License-out)迈向更高阶模式
2024年,中国药企海外授权交易总金额已突破500亿美元。在新的政策与国际化环境下,此类交易将持续火热,并呈现出新特点:交易标的将从单个上市产品,更多地向早期技术平台、前沿治疗领域(如多功能多肽、细胞治疗等) 延伸。合作模式也将从简单的销售权益授权,升级为包含联合研发、全球市场共拓的深度战略同盟。中国药企在全球产业链中的角色,正从“贡献者”向“定义者”悄然转变。
· 企业战略:从“本土化生存”到“全球化竞争力”构建
所有趋势最终将传导至企业战略层面。未来的成功药企必须具备两种核心能力:一是基于国内政策高效推进“研-审-用”闭环的敏捷执行力;二是以ICH等国际规则为基准,构建全球合规与临床开发体系的硬实力。市场也将加速分化,形成一批能驾驭全球研发、注册、商业化的“Big Pharma”,与众多在细分技术领域拥有绝对优势的“尖端Biotech”并存的健康生态。
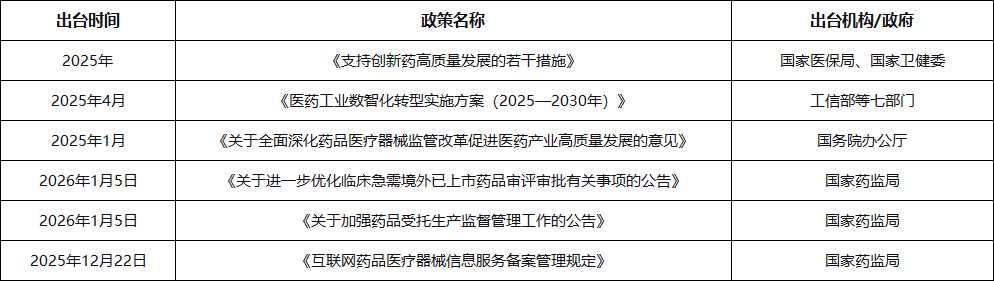
(部分相关政策)
结语
2025年的政策东风,并非简单的利好释放,而是一次深刻的产业制度性重构。它通过提供从研发到市场的“确定性”,为中国制药产业锚定了高质量发展的坐标。当国内高效的产业生态与全球通行的规则体系无缝衔接,中国创新药的全球竞争力将迎来一次质的飞跃。对于所有行业参与者而言,深刻理解并顺应这一确定性浪潮,是赢得未来的关键。