在生物药动辄每剂数千美元的今天,一次批次失败可能意味着数千万美元的损失。然而,绝大多数无菌制药工厂仍在用“手写记录+延时检测”的原始方式监控生产。本文深入剖析了从传统周期性监测向实时连续监控转型的技术路径,揭示了如何通过ATP生物发光、生物荧光粒子计数、多变量统计过程控制等前沿技术,将质量控制从“事后检验”推向“实时干预”,从而大幅降低报废率、提升GMP合规水平。
l 核心问题:目前,无菌处理过程中的分析技术应用严重滞后。
l 间歇式检测:大量参数仍依靠手持仪器或仪表盘读数进行周期性、非连续检测,无法实时捕捉异常。
l 数据孤岛:生产设备来自不同供应商,仪器间缺乏互联互通,软件不兼容,难以构建统一的制造管理系统。
l 结果滞后:传统微生物检测需数天培养周期,发现问题时,问题批次早已进入下一环节。
作者 Tony Cundell 博士尖锐指出:“可悲的是,目前的分析结果既未能有效实现实时无菌过程控制,也未能成功集成到制造管理系统中。”
过程分析技术的核心理念,是将控制点从成品检测大幅前移至生产过程中。通过在线、实时、数据驱动的决策,动态调整灌装参数甚至及时停机,从根本上减少报废、强化GMP绩效。
表一:无菌处理关键步骤与在线监测机会
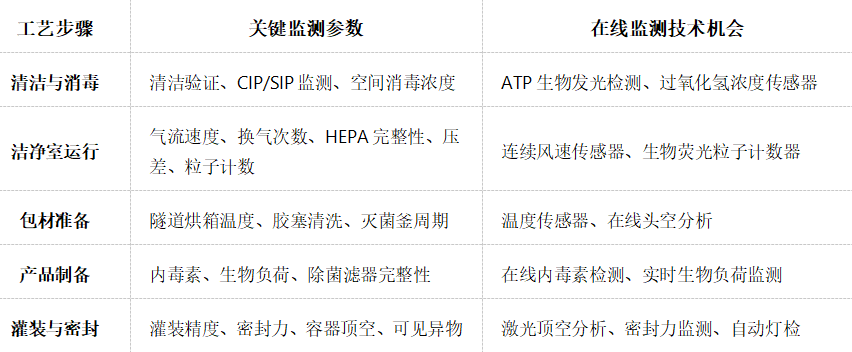
传统沉降菌培养需3-7天,而生物荧光粒子计数器通过405nm激光激发微生物自体荧光(如NAD(P)H、核黄素),可在实时区分并计数总颗粒与生物颗粒。
l 应用场景:洁净室动态空气监测、层析柱清洗监测、单抗下游工艺除菌过滤前生物负荷监测。
l 革命性价值:实时异常检测,无需等待实验室结果,实现真正的过程控制。
对于冻干产品(瓶内真空)或充氮保护产品,一旦胶塞密封不严,外界空气渗入即意味着产品失效。激光顶空氧分析仪可在线、无损检测瓶内氧气浓度变化,精度可达0%-25%,在贴标前100%剔除泄漏瓶。
源自食品工业的ATP检测,通过拭子取样、荧光检测,可在几分钟内量化表面残留的有机污染物(以相对光单位计)。尽管灵敏度不足以替代低菌落数检测,但作为清洁效果的即时判断工具,价值巨大。
胶塞的批间差异和老化效应会影响容器密封完整性。残余密封力监测虽不能直接预测泄漏,但与CCI高度相关。通过在线监测压塞后的残余密封力,可实时发现因组件尺寸偏差导致的密封不良。
无菌工艺涉及数十个相互关联的参数(风速、压差、粒子、温湿度等)。传统的单变量控制图无法揭示参数间的复杂关联。
l MSPC通过多变量统计模型,综合分析所有参数,生成多变量控制图。
l 应用案例:研究显示,手术室中非活性粒子、生物荧光粒子与活菌计数之间存在约0.7的中等相关性。MSPC可综合利用这些数据,在异常早期触发警报,甚至在仪表盘上给出优化建议。
美国FDA的cGMP法规明确要求,检测方法必须满足准确性和可靠性标准。
l 方法验证:非药典方法需按USP <1225>或<1223>进行验证。
l 仪器确认:遵循USP <1058>对A、B、C类仪器进行分类确认。
l 数据完整性:对GMP偏差和产品失败必须进行全面调查和纠正。
随着高价值生物药占比提升,批次失败的代价已无法承受。未来的无菌制造将是:
l 全数据驱动:所有关键参数通过无线传感器连续采集,无需人工干预(人工是主要污染源)。
l 智能分析:通过MSPC和机器学习,构建制造管理系统,在问题发生前预警,动态优化工艺参数。
l 终极目标:基于充分的过程监控数据,逐步替代部分成品放行检测,实现真正的实时放行。
Cundell 博士展望:“未来,过程监控数据或许将开始取代成品放行检测。构建一个基于过程监控数据、旨在防止产品失败、优化无菌处理多重输入的制造管理系统,是分析技术的总体目标。”
结语:
无菌制药的“黑箱”正在被实时监控技术一层层揭开。从“事后检验”到“实时干预”,不仅是技术升级,更是质量哲学的深刻变革。在这场工业4.0浪潮中,率先完成数字化转型的制药企业,将赢得质量、效率与成本的三重竞争优势。
(本文基于Tony Cundell博士发表于2026年3月4日的专业技术文章编译整理,原作者为Microbiological Consulting, LLC首席顾问)
