
复盘近年来的国家药监局飞检通报可以发现,数十款注射剂药品因未进行滤芯验证研究,屡屡被列为现场检查的重要缺陷项。这些案例时刻提醒着制药企业:过滤环节的合规性,已不容忽视。
在无菌药品生产中,除菌过滤是最后一道物理屏障。这道屏障一旦失效,后果不堪设想。然而,许多药企对过滤环节的关注,仍停留在“买个好滤芯”的浅层认知。当监管趋严、工艺复杂化、成本压力叠加时,过滤这道“看不见”的防线,正在成为影响药品质量、合规性与生产成本的关键变量。
飞检通报里的那些“雷”,已经替大家踩过了。现在的问题是:你的过滤系统,经得起下一次检查吗?

01“看不见"的风险,正在成为“看得见"的缺陷
在无菌药品生产中,除菌过滤系统的完整性直接决定产品能否免受微生物污染。然而,这一环节却隐藏着多重系统性风险。
完整性风险是首要挑战。滤芯若存在微小缺陷,可能导致微生物泄漏。更棘手的是,常规的泡点测试或扩散流测试属于非破坏性物理测试,其检测结果与细菌截留能力相关,但并不能完全等同于对微生物泄漏的绝对判断。一旦完整性测试出现偏差,整批次产品便面临污染风险。
材质相容性风险同样不容忽视。劣质或不匹配的滤材,可能释放可提取物和浸出物,污染药液。根据国家药监局发布的《除菌过滤技术及应用指南》,除菌过滤工艺验证应包含化学兼容性试验、可提取物或浸出物试验等内容,企业需在过滤系统验证中完成相关研究。
验证不足风险则直接影响合规性。针对特定料液,若缺乏细菌截留试验、化学兼容性试验、吸附试验等完整验证数据,工艺验证便存在盲区。当监管部门检查时,这往往成为关键缺陷项。
02监管划了哪些红线?药企必须知道的“硬指标”
近年来,国内药品监管体系正加速与国际接轨,对无菌药品生产中的过滤环节提出了更为严格的要求。
现行《药品生产质量管理规范》(GMP)无菌药品附录明确要求,除菌过滤器的完整性应在使用前和使用后进行测试,过滤除菌工艺应当经过验证,验证中应当确定过滤一定量药液所需时间及过滤器两侧的压力。同时,同一规格和型号的除菌过滤器使用时限应当经过验证,一般不得超过一个工作日。这些条款构成了过滤验证的基本框架。
2018年,国家药监局发布的《除菌过滤技术及应用指南》进一步细化了相关要求。该指南强调,企业应建立过滤器验证的完整档案,包括细菌截留试验、化学兼容性试验、可提取物/浸出物研究等;对于关键工艺环节的除菌过滤器,应实施冗余过滤策略;过滤器更换周期应根据验证数据确定,而非简单地“定期更换”。
值得关注的是,国内监管检查的重点正从“是否使用除菌过滤器”向“过滤系统的验证是否科学、完整”转变。在药品注册核查中,与过滤系统验证相关的缺陷项持续受到关注。
03为什么通用滤芯,越来越“不够用"了?
随着制药工艺的快速发展,过滤环节面临的挑战也在不断升级。不同剂型、不同料液对过滤方案提出了差异化的技术要求。
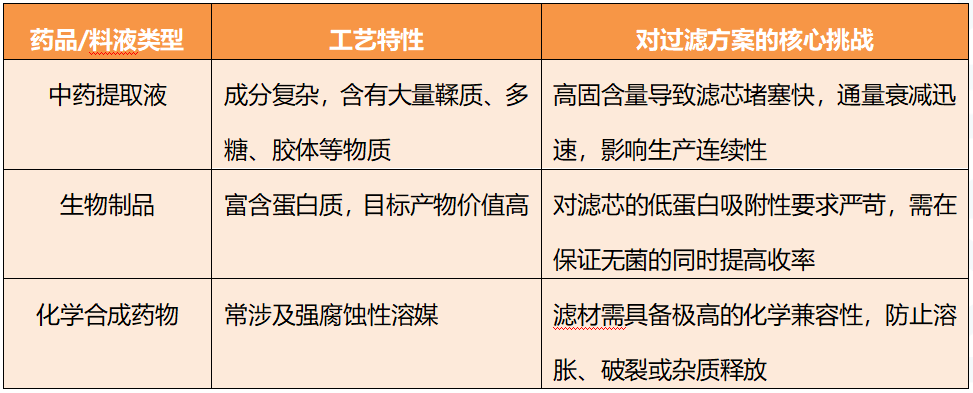
这些挑战意味着,通用型过滤方案已无法满足现代制药工艺的多样化需求。从成分复杂的中药提取液、富含蛋白的细胞培养液到强腐蚀性的合成溶媒,不同料液对滤芯的化学兼容性、蛋白吸附性和通量稳定性提出了差异化要求,精准匹配成为必然选择。
04破局之道:国产高端过滤的崛起与验证体系
面对上述风险与挑战,制药企业亟需一套系统性的过滤解决方案——不仅需要可靠的滤芯本身,更需要权威的验证数据和全流程的技术支持。在这一领域,以零界净化为代表的国产高端过滤品牌,正在实现从“可用”到“可信”的跨越。
零界净化的技术突破始于核心膜材的自主研发。其PES微孔滤膜采用高度不对称结构设计,既能通过预过滤层显著提升纳污量,又能依靠精密截留层保证对细菌等微生物的绝对拦截。这意味着什么?简单说,换一次滤芯,能处理的料液更多;处理同样量的料液,换芯次数更少。
实际测试数据显示,在发酵液过滤中,该滤膜的最大载量达到10,000 L/m²。在制造工艺层面,零界净化应用特殊的滤膜打折工艺,其V型打折工艺可将10英寸滤芯的过滤面积从0.55㎡提升至0.75㎡,而月牙型打折工艺则能将面积增加至1.0㎡,显著增强了单支滤芯的处理能力。
更为关键的是,零界净化是国内少数拥有中国合格评定国家认可委员会(CNAS)认可实验室的滤芯供应商。该资质标志着其检测能力已达到国家与国际标准,能够提供贯穿产品全生命周期的质量保障。对于制药企业而言,这意味着在应对监管审计时,能够提供具有公信力的完整验证档案。
验证能力的构建,既需要硬件端的可靠支撑,也离不开行业知识体系的持续输入。当前,国内监管正加速与国际标准接轨,企业对验证前沿方法的掌握变得愈发关键。值得一提的是,由徐禾丰老师带队翻译的《制药工艺验证手册》第四版中文版已成为验证领域的重要参考资料,可作为企业完善验证知识体系的重要参考。


05生态协同:国产过滤的群体性突破
零界净化的突破并非孤例,而是中国制药装备行业整体升级的缩影。在过滤细分领域,一批国产企业正在形成群体性突破。
在膜材料领域,国产企业已成功研发出应用于除菌过滤的PVDF微孔滤膜,其性能指标达到国际先进水平。在系统集成层面,部分制药装备企业在其一次性生物反应器系统中全面采用国产除菌过滤组件,实现了从“设备+耗材”的整体国产化替代。
这些案例共同指向一个结论:国产高端过滤产品已具备与国际品牌同台竞技的实力,制药企业在关键耗材上有了更具性价比、更可控的战略选择。
06价值重构:从“成本项”到“价值点”的战略升级
对于制药企业而言,选择经过充分验证的国产高端过滤方案,已不仅是成本考量,更是系统性管控风险、提升竞争力的战略选择。
在质量与合规层面,具备CNAS实验室验证支持的过滤方案,能显著加速产品注册与现场审计进程。当监管机构问及“你的过滤系统是否可靠”时,完整的验证档案就是最好的答案。
在综合成本层面,高性能过滤带来的价值清晰可见。相较于进口品牌,国产高端替代提供了更具竞争力的采购价格;高纳污量设计大幅延长更换周期,减少非计划停机带来的产能损失;对于生物制品而言,低蛋白吸附特性直接关联收率提升,转化为经济效益。
在供应链安全层面,作为本土企业,国产过滤品牌能够提供更快的响应速度、更灵活的技术服务。在当前全球供应链波动加剧的背景下,与本土高端耗材商形成战略协同,能有效增强供应链的韧性和自主可控能力。
当越来越多像零界净化这样的中国过滤企业,能够用自主创新的膜材料、CNAS认可的验证能力和全场景覆盖的产品矩阵,为药企提供“质量可验证”的过滤解决方案时,中国制药工业的质量防线将更加坚实,全球竞争的底气也将更加充足。这不是简单的“国产替代”,而是基于质量自信的“全球优选”。
文中数据及参数均由企业提供,如果您对产品感兴趣,请在后台留下姓名、单位及联系方式,相关人员会与您联系。 转载请至公众号后台留言申请开白,文章需在允许范围内使用,原则上文章标题、内容不可进行修改、删减,排版方面可依据账号排版风格改动。